Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Médica La Paz
versão On-line ISSN 1726-8958
Rev. Méd. La Paz v.16 n.2 La Paz 2010
EDUCACIÓN MÉDICA CONTÍNUA
REVISIONES SISTEMÁTICAS (1)
Dr. Raúl Arturo Arévalo Barea*, Dr. Gonzalo Ortuño**, Univ. Dory Esther Arévalo Salazar***
* Diplomado Medicina Basada Evidencia, Revisiones Sistemáticas, Metodología Investigación, Elaboración Guías Clínicas
** Coordinador Carrera de Fisioterapia - UNICEN
*** Estudiante Carrera de Medicina - UMSA
Responsable: Dr. Raúl Arévalo Barea. E-mail: luar999@hotmail.com
INTRODUCCIÓN
Las Revisiones Sistemáticas (RS) son cada vez más la fuente de información actualizada en la aplicación de decisiones clínicas, que logren la mejoría en los pacientes en los que se apliquen las mismas. Las RS se pueden realizar para situar los problemas en una situación comparativa y lograr describir los daños probables de cada una de las conclusiones que se alcanzan. Se ha constituido como una herramienta que colabore con la interpretación de los significados que los individuos o grupos les asignan a un problema, cómo y por qué funcionan las opciones, y los puntos de vista y las experiencias de las partes interesadas (stakeholders) relacionados con las opciones en particular. Una serie de limitaciones ha impedido el uso más generalizado de revisiones sistemáticas en la toma de decisiones. Esto incluye una falta de conciencia del valor y una falta de coincidencia entre los términos utilizados por los responsables de la toma de decisiones en políticas, al intentar recuperar las revisiones sistemáticas, y los términos utilizados por los autores originales de esas revisiones. La falta de coincidencia entre los tipos de información que buscan los responsables de la toma de decisiones en políticas y la manera en la que los autores fallan en resaltar (o hacer obvia) esa información dentro de las revisiones sistemáticas también resultaron problemáticas. En este artículo, sugerimos tres preguntas que se pueden utilizar para orientar a quienes buscan revisiones sistemáticas, particularmente revisiones sobre los impactos de las opciones que se están considerando. Estas son:
1. ¿Es realmente una revisión sistemática lo que se necesita?
2. ¿Qué bases de datos y estrategias de búsqueda se pueden utilizar para buscar revisiones sistemáticas relevantes?
3. ¿Qué alternativas están disponibles cuando no se puede encontrar ninguna revisión relevante?
REVISIÓN SISTEMÁTICA
Una RS reúne toda la evidencia empírica que responde criterios de elegibilidad previamente establecidos, para responder una pregunta específica de investigación. Utiliza métodos sistemáticos y explícitos, que se eligen con el fin de minimizar y eliminar sesgos, brindando así resultados confiables a partir de los cuales se puedan extraer conclusiones y tomar decisiones.
ESTRUCTURA DE UNA REVISIÓN SISTEMÁTICA
Son búsquedas sistemáticas que identifican todos los estudios que puedan cumplir los criterios de elegibilidad.
Utilizan metodología explícita y reproducible.
Presentan un conjunto de objetivos claramente establecidos, con criterios de elegibilidad de estudios previamente definidos.
Realizan evaluaciones de la validez de los resultados de los estudios incluidos, mediante la evaluación del riesgo de sesgos.
Son presentaciones sistemáticas, que incluyen una síntesis de las características y resultados de los estudios incluidos.
Muchas de las revisiones sistemáticas contienen metanálisis. El metanálisis consiste en la aplicación de métodos estadísticos para resumir los resultados de estudios independientes (Glass 1976). Al combinar la información de todos los estudios relevantes, el metanálisis puede obtener estimaciones más precisas de los efectos sobre la atención en salud que las derivadas de los estudios individuales incluidos en una revisión.
TIEMPOS LÍMITES
Los clínicos, los usuarios y pacientes, los investigadores y todas aquellas personas que integran y son parte de las políticas en salud afrontan cantidades enormes de información concerniente a evidencia en investigación biológica. Es reconocido que los del equipo de salud cada vez cuentan con menor tiempo, con menos habilidades y con los recursos técnicos para encontrar, interpretar e evaluar la evidencia e incorporarlas a las decisiones que beneficien a los usuarios de los servicios de salud.
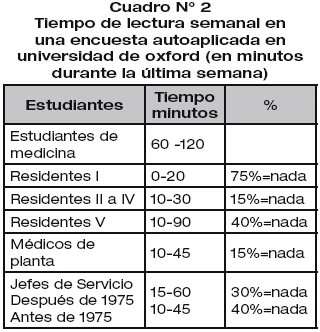
Las encuestas que se han realizado sobre el tiempo que empleamos a buscar información para mejorar la toma de decisiones en relación a nuestros pacientes, encontrándose que el tiempo es muy corto. Si consideramos los trabajos de investigación que evalúan el tiempo que dedican los estudiantes de de medicina, los residentes, los médicos de planta e incluso los jefes de Servicio a ampliar la información sobre sus pacientes se encuentran resultados con cifras bajas y cuando se analiza la relación entre el tiempo dedicado a buscar información y el dedicado a leerla, se encuentra que los tiempos son poco menos que espectaculares. Además si no se está conectado a una red con posibilidades de acceder a la información, el tiempo que se invierte en identificar los artículos, bajarlos y llegar a fotocopiarlos, es enorme y esto se convierte en un verdadero acto heroico (Cuadro N° 1 y N° 2)

Las respuestas buscadas las podemos encontrar en las RS que la Colaboración Cochrane (CC) pone a disposición de forma libre y sin costo, identificando, evaluando y sintetizando la evidencia basada en la investigación y presentándola en un formato comprensible. La CC prepara, mantiene y fomenta la difusión de RS para fundamentar decisiones relacionadas con la atención sanitaria (revisiones Cochrane).
Las revisiones sistemáticas (RS) son consideradas en el momento el origen de información acertada para la buena toma de decisiones en el área de salud. Las RS tienen las siguientes ventajas sobre las investigaciones individuales al identificar los impactos de una iniciativa:
Son investigaciones sistematizadas, con un alto nivel de validación y calificación (eliminan los sesgos), por lo que reducen la probabilidad de que los responsables de la toma de decisiones en políticas de salud sean incitados a errores por parte de las investigaciones.
Aumentan la confianza entre los dispensadores de salud en la toma de decisiones acertadas, mediante la aplicación de las evidencias encontradas, con disminución de los sesgos y aumento en la precisión de los datos.
Permiten realizar la búsqueda de evidencias de revisiones sistemáticas propias (en lugar de tener que buscar y sintetizar la evidencia de la investigación disponible por su propia cuenta).
Las RS también permiten a los responsables de la toma de decisiones en políticas de salud centrarse en la recolección y síntesis de otros tipos de evidencia, como la evidencia local sobre la viabilidad técnica, la adaptación a los problemas dominantes en el ámbito multicultural (rural/urbano) del momento, y la aceptabilidad de las opciones posibles en términos de viabilidad del presupuesto y del proceso de implementación respaldada políticamente por los entes gestores de salud y economía.
Permiten la aceptación, y rechazo de las partes interesadas en salud, como también la sociedad civil.
Las RS de impacto incentivan a la realización de los metanálisis y por ende de las investigaciones científicas primarias y secundarias.
Además de las cada vez más eficientes maneras de encontrar, clasificar y almacenar la información, aplicando además estrategias para elegir aquéllas de utilidad, y separarlas de las no válidas o no aplicables, los dispensadores de salud se enfrentan al problema de la producción exponencial de la literatura, haciéndose imposible, revisar todos los artículos que respondan una pregunta clínica, más aún cuando muchas son las veces que muchos de ellos llegan a conclusiones relevantes sobre la misma cuestión.
También es adecuado señalar que las RS son artículos científicos en salud (medicina) que siguen una metodología explícita para resumir la información sobre determinado tema o problema de salud. Se diferencia de las Revisiones Narrativas (RN) en que provienen de una pregunta estructurada y de un protocolo previamente realizado. Además la búsqueda de la evidencia se ha desarrollado de manera sistemática con una declaración de los criterios de selección y se ha hecho una evaluación crítica de los artículos primarios y una síntesis basada en la calidad metodológica de los estudios. Cuando una RS termina en un estimador estadístico se denomina metanálisis.
En las revisiones narrativas el criterio para incluir o excluir artículos depende en gran medida del punto de vista del autor, que en este tipo de revisiones suele no tener en cuenta la calidad metodológica ni el tamaño muestral de los estudios. Además al no existir una estrategia sistemática de búsqueda, es muy probable que estudios importantes que podrían modificar las conclusiones en forma significativa no sean incluidos en la revisión.
La metodología para la realización de una RS puede ser encontrada en las publicaciones de Cochrane Handboock producida por la Colaboración Cochrane; y en el CDR Report producido por el NSH Centre for Reviews and Dissemination Las revisiones Cochrane se publican en línea a texto completo en la Base de Datos Cochrane de Revisiones Sistemáticas (Cochrane Database of Systematic Reviews, CDSR, sigla en inglés), que es un componente básico de The Cochrane Library. The Cochrane Library está publicada por Wiley-Blackwell en Internet (www.thecochranelibrary.com), y es accesible de forma gratuita para nuestro país gracias al acceso libre que provee Wiley-Blackwell. En otros lugares se requiere suscripción o pay-per-view.
OBJETIVO
El objetivo de las RS es reunir toda evidencia que se corresponda con unos criterios de elegibilidad establecidos previamente, con el fin de orientar un tema específico de investigación.
PROPÓSITO
El propósito de las RS es minimizar sesgos mediante la aplicación de métodos sistemáticos y explícitos.
Diferencias entre revisión sistemática y revisión narrativa


QUE DEBEMOS TENER EN CUENTA
Las siguientes cuestiones pueden orientar a los miembros del equipo de salud (clínicos, quirúrgicos, bioquímicas, enfermeras, psicólogas, fisioterapistas, fonoaudiólogas, administradores y gerentes) para la toma de decisiones:
LAS REVISIONES SISTEMÁTICAS SON UNA SOLUCIÓN
Las RS pueden proporcionar información útil que se relacionen con la mejor atención en salud, la mejor respuesta a las preguntas en cuestión que se relacionen con los Servicios, medicamentos, soluciones del sistema de salud, e incluso en las estrategias de implementación.
Son un aporte en la consolidación de la aplicación de los principios activos, veremos las siguientes evidencias:
EVIDENCIA 1: Qué tenemos entendido en relación a que la terapia antirretroviral reduce el riesgo de transmisión vertical de la infección por virus de la inmunodeficiencia humana VIH.
A finales de 1998, había más de 33 millones de personas infectadas con el virus de inmunodeficiencia humana (VIH) y más de un millón de niños que habían sido infectados por sus madres. El objetivo de esta RS fue evaluar qué intervenciones podrían ser efectivas para disminuir el riesgo de transmisión materno-infantil de la infección por VIH, así como su efecto en la morbimortalidad materna y neonatal. La Estrategia de búsqueda se realizó a partir de los registros de ensayos del Grupo Cochrane de Embarazo y Nacimiento (Cochrane Pregnancy and Childbirth Group) y en el Registro Cochrane de Ensayos Controlados (Cochrane Controlled Trials Register). Se utilizaron como criterios de selección las pruebas aleatorizadas que comparaban cualquier intervención encaminada a reducir el riesgo de transmisión vertical de VIH con el uso de un placebo o ningún tratamiento, o cualquier conjunto de dos intervenciones o más que buscaran reducir el riesgo de transmisión vertical de este tipo de infección. Los resultados principales encontrados fueron los siguientes:
En relación a la Zidovudina (zdv): Se incluyeron cuatro estudios en los que se comparó la zdv y un placebo, se incluyeron 1.585 mujeres. Comparado con el placebo, se registró una reducción significativa en el riesgo de transmisión vertical mediante el uso de cualquier zdv (riesgo relativo (RR) 0.54, intervalo de confianza (IC) 95%, 0.42-0.69). No se encontró evidencia de que el tratamiento largo sea superior al "régimen corto".
No se encontró evidencia de heterogeneidad significativa entre pruebas y no se han hecho comparaciones directas aleatorizadas entre el tratamiento largo y el corto. Por lo tanto, no está claro si el tratamiento largo es superior al corto, en cuanto a la reducción del riesgo de transmisión vertical del VIH. Además, se puede notar que la magnitud de dicho riesgo es similar en poblaciones donde la mayoría de las mujeres amamanta (RR 0.62, IC 95% 0.46 - 0.85) y en poblaciones donde las madres no amamantan (RR 0.50, IC 95% 0.30 - 0.85). La incidencia de transmisión en los grupos de tratamiento y placebo es más elevada en poblaciones que amamantan que en las que no amamantan, pero la reducción del riesgo relativo en la transmisión es similar en ambas poblaciones. Parece ser también que la zdv disminuye el riesgo de muerte neonatal (RR 0.31, IC 95% 0.11 - 0.90) y el número de muertes después del periodo neonatal (RR 0.46, IC 95% 0.24 - 0.90). Aparentemente, la zdv no tiene efecto sobre la incidencia del alumbramiento prematuro, peso al nacer o muertes maternas.
En relación a la Nevirapina (nvp): Un ensayo comparó nvp intraparto y postnatal con zdv intraparto y postnatal en 626 mujeres, la mayoría de las cuales amamantó a sus bebés. Comparándola con la zdv, se encontró una reducción significativa en el riesgo de transmisión vertical del VIH al usar nvp (RR 0.58, IC 95% 0.40-0.83). No existen pruebas disponibles en las que se compare la nvp con un placebo.
Una prueba grande, bien realizada, controlada y aleatorizada, sobre el uso de la nvp demuestra claramente la efectividad de dicho medicamento para prevenir la transmisión vertical del VIH comparada con el uso de zdv intraparto y posparto (RR 0.58, IC 95% 0.40-0.83). La toxicidad de ambas intervenciones parece ser similar y poco frecuente.
En relación a la Cesárea: Se incluyó una prueba que comparaba cesárea programada con expectativa de alumbramiento vaginal, con la participación de 436 mujeres. Al compararla con el parto vaginal, se observó una reducción significativa en el riesgo de transmisión vertical de infección por VIH con la cesárea (RR 0.17, IC 95% 0.05-0.55). Sólo una prueba controlada y aleatorizada ha comparado la cesárea programada con la expectativa de alumbramiento vaginal, lo que demuestra una marcada reducción en el riesgo de transmisión con la cesárea programada (RR 0,17, IC 95% 0,05 - 0,55). No se encontró evidencia de complicaciones posparto significativas en ningún grupo de esta prueba.
CONCLUSIONES
De acuerdo a lo analizado tenemos las siguientes conclusiones que avalan las acciones en las mujeres embarazadas que viven con el VIH y que no transmitan a sus productos el virus. Cómo se utilizará la evidencia obtenida a partir la las investigaciones clínicas aleatorizadas depende del escenario dentro del cual se atienda a las mujeres infectadas por VIH. En países industrializados, la práctica se ha empezado a modificar a partir de la evidencia actual y parece ser que la terapia antirretroviral combinada es el estándar de atención. Además, aparentemente muchos centros ofrecen el alumbramiento por cesárea programada, con la esperanza de que ello reducirá más el riesgo de transmisión. En nuestros países en vías de desarrollo, el uso de un tratamiento corto con zdv y el de dosis única de nvp parecen ser terapias efectivas. Ahora el reto es instituir esta terapia en la práctica. El uso generalizado de la cesárea programada es una opción adecuada.
La estrategia se realizó en el registro de estudios clínicos del Grupo Cochrane de Embarazo y Parto (Cochrane Pregnancy and Childbirth Group) y el Registro Cochrane de Estudios Clínicos Controlados (Cochrane Controlled Trials Register). También realizarón el análisis de los resúmenes de los congresos internacionales sobre SIDA (International AIDS Conferences) y congresos sobre Retrovirus e Infecciones Oportunistas(Conference on Retroviruses and Opportunistic Infections).
Alcanzandose las siguientes conclusiones por los autores: Esta revisión permite concluir que la monoterapia corta con Zidovudina y la monoterapia corta con nevirapina.
EVIDENCIA DOS: Qué evidencias tenemos sobre uno de los problemas que cada vez es más importante como la sífilis congénita en relación al antibiótico para la sífilis diagnostica durante el embarazo.
La magnitud del problema de la infección por el Treponema pallidum, las tasas de sífilis informadas varían ampliamente de un país a otro. Las tasas correspondientes a países industrializados están mejor documentadas, en tanto que existe menos información respecto de los países en vías de desarrollo, donde la enfermedad está más diseminada. Por ejemplo, en algunas regiones de África: 360 cada 100.000 habitantes (Hook III 1992).
La infección se puede transmitir verticalmente de una embarazada infectada al feto y al menos dos tercios de todos los neonatos de mujeres con sífilis que no recibieron tratamiento resultan infectados (Zenker 1990). Sin embargo, el riesgo para el feto o neonato varía considerablemente según el estadio de la sífilis sin tratar que atraviese la madre (Ingall 1990). Los antecedentes obstétricos generales de una mujer con sífilis que no recibe tratamiento (que se conoce como ley de Kassowitz) dictan que los primeros embarazos terminan en aborto o mortinato, los embarazos posteriores, en neonatos a término con sífilis congénita y las paridades mucho mayores en neonatos no afectados por la enfermedad. En otras palabras, la evolución natural, en cuanto al resultado perinatal, de la sífilis no tratada en mujeres es que la inefectividad y severidad se atenúan con cada embarazo sucesivo (Ingall 1990; Schulz 1992).
La sífilis congénita es un trastorno grave que, si no provoca la muerte a temprana edad, puede causar trastornos permanentes, debilidad y desfiguración como consecuencia de los estigmas asociados a esta enfermedad. El estado clínico de la dificultad del crecimiento puede estar correlacionado con el hallazgo patológico frecuente de pancreatitis aguda e inflamación del tracto gastrointestinal (Ingall 1990). La sífilis congénita es un problema cada vez más importante en muchos países en vías de desarrollo y en las economías de transición de Europa Oriental y la ex Unión Soviética. En varios países, este aumento se ha visto agravado por el VIH/SIDA. Si bien la efectividad de la penicilina en el tratamiento de la sífilis en embarazadas y la prevención de la sífilis congénita se estableció poco tiempo después de la introducción de la penicilina en la década de 1940, aún para 2011 no se conoce con certeza cuáles son los regímenes terapéuticos óptimos de tratamiento antibiótico más efectivo (en lo que respecta a la dosis, la duración del ciclo y la vía de administración) para la sífilis con y sin infección concomitante con VIH para embarazadas infectadas por sífilis.
La estrategia de búsqueda fue a partir de MEDLINE tomando desde el 1966 hasta octubre de 2002; EMBASE 1974 hasta marzo de 2000, el Registro Cochrane de Estudios Clínicos Controlados (Cochrane Controlled Trials Register), el registro de estudios clínicos del Grupo Cochrane de Embarazo y Parto (Cochrane Pregnancy and Childbirth Group) y las referencias de las revisiones tradicionales, además se contacto con expertos en unidades de especialistas en diferentes países
CONCLUSIONES: Los resultados de la RS considera que si bien no hay dudas de que la penicilina es efectiva en el tratamiento de la sífilis durante el embarazo y la prevención de la sífilis congénita, aún no se sabe con certeza cuáles son los regímenes terapéuticos óptimos. No se identificó estudio clínico controlado como guía al decidir si se deben modificar los regímenes terapéuticos recomendados del tratamiento antibiótico (penicilina) para embarazadas con sífilis. Se necesitan estudios adicionales para evaluar los casos de fracaso del tratamiento con los regímenes recomendados actualmente y éstos deberían incluir una evaluación del papel que juega la infección por VIH en los casos de fracaso del tratamiento en sífilis prenatal. La efectividad de diversos regímenes de antibióticos para el tratamiento de la sífilis primaria y secundaria en embarazadas debe ser evaluada mediante estudios clínicos controlados aleatorizados que los comparen con las recomendaciones actuales. La acción recomendada para las autoridades que dispensan salud es la necesidad de realizar un estudio colaborativo que establezca cuáles son los regímenes terapéuticos óptimos.
LA BÚSQUEDA DE LAS RS RELEVANTES SE LAS ENCUENTRA
La RS que debe abordarse se relaciona con la mejor atención en salud, se pueden encontrar en la base datos CC plus, se puede acceder a ella sin costo, tiene un enfoque particular en sus conclusiones sobre la práctica clínica y sobre las implicaciones para la investigación científica. La base de datos captura revisiones sistemáticas que abordan preguntas sobre los impactos y las revisiones sistemáticas que abordan otros tipos de preguntas. La Biblioteca Cochrane, y específicamente la Base de Datos Cochrane de Revisiones Sistemáticas y la Base de Datos de Resúmenes de Revisiones de Efectos, Medline Plus, BIREME.
LAS RS SE HALLAN DE FORMA PERMANENTE
El Registro Central Cochrane de Ensayos Controlados (The Cochrane Central Register of Controlled Trials, CENTRAL) contiene información bibliográfica de cientos de miles de ensayos controlados, e incluye también informes publicados en resúmenes de conferencias y otras fuentes no incluidas en otras bases de datos bibliográficas.
La Base de Datos Cochrane de RS (Cochrane Database of Systematic Reviews, CDSR) contiene los textos completos (que incluyen métodos, resultados y conclusiones) de las revisiones y protocolos Cochrane.
La Base de Datos de Resúmenes de Revisiones de Efectos (Database of Abstracts of Reviews of Effects, DARE) compilada y mantenida por el Centro de Revisiones y Divulgación (Centre for Reviews and Dissemination) de York, Reino Unido, incluye evaluaciones críticas y resúmenes estructurados de otras revisiones sistemáticas que cumplen unos criterios de calidad explícitos.
El Registro Cochrane de Metodología (Cochrane Methodology Register) contiene información bibliográfica de artículos y libros en el campo de la investigación en revisiones, así como un registro prospectivo de estudios metodológicos.
ELABORACIÓN DE UNA REVISIÓN SISTEMÁTICA
REDACTAR UN TÍTULO PARA LA REVISIÓN SISTEMÁTICA SIGUIENDO EL FORMATO ESTANDARIZADO
Redactar un título para la revisión sistemática siguiendo el formato estandarizado de las revisiones Cochrane. Este formato establece una formulación básica para los títulos.
La elaboración de los títulos de forma provisional podrán ser reformulados y refinado en las etapas posteriores, según se avance en el proceso de registrar el protocolo de RS.
COMPROBAR QUE LA REVISIÓN YA SE REALIZÓ
Se debe investigar si hay otras personas desarrollando una RS que coincida o se parezca con otras revisiones. En esta situación, se debe consultar la página web donde se encuentren las listas de todas las RS concluidas, asi como las que todavía no están publicadas en las librerías de bases electrónicas conocidas. (ej.: http://www.cochrane.no/titles/). Cuando la RS se encuentre ya registrada por algún grupo, será necesario plantear otra propuesta de RS. El Grupo Cochrane de Revisión (GCR) también tiene un registro de títulos que se puede consultar.
REGISTRAR EL TÍTULO DE REVISIÓN EN EL GRUPO COCHRANE DE REVISIÓN CORRESPONDIENTE
Enviar un correo electrónico al editor coordinador del grupo, proponiendo el título de revisión que se desea registrar. En esta dirección se puede encontrar una lista de todos los CRG, con sus datos de contacto y su página web, si tienen: http://www.cochrane.org/contact/entities.htm#CRGLIST
CONTACTAR CON EL CENTRO COCHRANE DEL INSTITUTO DE EFECTIVIDAD CLÍNICA Y SANITARIA (IECS) / CENTRO COLABORADOR DE LA RED COCHRANE IBEROAMERICANA
Realizado el registrado del título, o en el supuesto caso que aparezcan algún problema o duda durante el proceso, se podrá escribir un correo electrónico al Centro Cochrane del IECS (cochrane@iecs.org.ar) que indique el título de revisión registrado o por registrar. La persona responsable del apoyo logístico y metodológico a los revisores, entrará en contacto con el grupo que está realizando la RS para proporcionar información adicional si es necesario.
LEER EL MANUAL DE ELABORACIÓN DE RS
Existen varios manuales y guías en ingles que conducen la elaboración de las RS, habiendo en el momento una versión traducida al castellano del manual elaborado por la Colaboración Cochrane, donde se encuentran explicados los conocimientos y los pasos adecuados para poder realizar las RS. La página que se sugiere visitar inicialmente es: http://www.cochrane.es/Castellano/CC_Handbook, donde se encuentra el archivo en formato Word
ASISTIR A UN CURSO DE FORMACIÓN DE NIVEL INTERMEDIO-ALTO
Es recomendable asistir a un curso de formación presencial "Curso Universitario de Postgrado": Revisiones Sistemáticas y meta-análisis, que es impartido por el Centro Cochrane del IECS. Se recomienda realizar consultas sobre la agenda de cursos en la página: http://www.iecs.org.ar/iecs-visor
La mayor parte de las veces esto significa un tiempo adicional y un costo económico, por lo que se puede inscribir en el curso interactivo "Curso electrónico de Revisiones Sistemáticas", visitando la página: (http://www.cochrane.es/Cursos/RevSys_curs) donde se pude adquirir y realizar practicas con la metodología "paso a paso", adquiriendo los conocimientos y habilidades suficientes pero necesarias para realizar una RS, durante el curso se realizan evaluaciones de cada uno de los módulos, y se certifica de la conclusión del mismo. (no tiene costo, excepto el uso de su PC).
DESARROLLO DE UNA RS
Una vez concluido el protocolo debe seguir el paso de la publicación y el lugar recomendado es a nivel de la Base de Datos Cochrane de Revisiones Sistemáticas, se envía el contenido donde previamente a la publicación de la revisión CC, aportar para reducir el impacto de sesgos de los autores, fomentan la transparencia de los métodos y los procesos planteados, analizan la posibilidad de duplicación, y permite la revisión por pares de los métodos planificados.
JUSTIFICACIÓN DE LOS PROTOCOLOS
Elaborar una RS tiene su dificultad porque involucra muchos juicios. Debiéndose considerar como máxima prioridad en todo el proceso la disminución potencial de sesgos, se debe evitar influenciar o dejarse influenciar, en el criterio subsecuente de la elegibilidad del estudio, la elección de las comparaciones a evaluar entre intervenciones, o las variables de resultado a publicar en la revisión. Una vez iniciada la RS se debe mantener constante al protocolo de revisión publicado, a veces los cambios en estos protocolos son necesarios. Esta situación es similar a la de un protocolo para un ensayo aleatorizado, que algunas veces debe ser cambiado para adaptarlo a circunstancias imprevistas, como problemas de inclusión de los participantes, la extracción de datos, o la incidencia de eventos inesperados.
FORMATO DE UNA REVISIÓN
El formato que utiliza CC se adapta a los diferentes tipos de revisiones, por ejemplo las que hacen una única comparación, las que realizan múltiples comparaciones y las que analizan datos de pacientes individuales.
Es recomendable para poder facilitar el esquema de trabajo utilizar el formato que utiliza Cochrane en todas sus revisiones, el mayor beneficio por su practicidad incluye:
a) Ayuda a los lectores a encontrar rápidamente los resultados de la investigación y a evaluar la validez, la aplicabilidad y las implicaciones de esos resultados;
b) Es una guía para los autores de la revisión a informar sobre su trabajo de forma explícita y concisa, y minimizar el esfuerzo requerido para hacerlo;
c) Facilitar la publicación electrónica y el mantenimiento de las revisiones;
d) Posibilitar el desarrollo de productos derivados y estudios empíricos basados en múltiples revisiones sistemáticas.
PROPÓSITOS PARA HACER UNA REVISIÓN
El propósito para elaborar una RS puede ser generada por resolver una discusión que puede establecerse después de una visita médica conjunta en un Servicio clínico, o en algunos casos si se trata de resolver una controversia en un tratamiento o cuando se intente responder preguntas que se generan cuando la práctica clínica es incierta, en el caso de explorar variaciones en la práctica clínica, confirmar la eficacia de una práctica determinada o destacar un tema para una investigación futura.
El objetivo general de una RS debe:
1. Compendiar y ayudar al colectivo docente de salud a entender la evidencia científica
2. Deben permitir al equipo multidisciplinario la toma adecuada de decisiones prácticas sobre la atención de los pacientes
3. Ayuda a resolver situaciones de dualismo interpretativo sobre diferentes razones clínicas y/o quirúrgicas mediante la decisión de utilizar una RS Cochrane o se hace una revisión local
La utilidad de las RS debe alcanzar a las autoridades que toman las decisiones sobre la atención en salud.
El mayor logro es haber obtenido los resultados que aportarán la mejor evidencia actual sobre la cual basar las decisiones, y deben ser descritos con suficiente detalle en el protocolo para que los lectores puedan comprender adecuadamente los pasos planeados. De la misma manera se hace muy importante que se conozca cuando la evidencia no es fiable o en muchas ocasiones no hay evidencia científica sobre determinadas variables de resultado que puedan ser importantes para los que toman las decisiones.
EL EQUIPO DE REVISIÓN
El Equipo de revisión asegura que las labores como la selección de estudios para elegibilidad y la extracción de datos puedan ser realizadas independientemente por al menos dos personas, aumentando así la posibilidad de detectar errores. Los equipos de RS deben tener expertos en el área temática que se está revisando e incluyen, expertos en la metodología de las revisiones sistemáticas.
El trabajo en las RS con el transcurso del tiempo da la experiencia en el proceso de revisión sistemática y los de mayor conocimiento deben trabajar con los menos expertos y sobre todo alentar a participar en los talleres de formación, que organiza la Colaboración Cochrane.
SOFTWARE PARA AUTORES DE REVISIÓN Y APOYO EDITORIAL A LOS GRUPOS DE REVISIÓN SISTEMÁTICA
Hay el software para autores de RS que apoyan en la preparación y la supervisión editorial. También se tiene Dirección del Sistema de Información (IMS). El IMS tiene dos componentes principales: un software para la redacción de las revisiones, Review Manager (RevMan), y un servidor central para el manejo de documentos y los datos de contacto, Archie.
RECURSOS PARA UNA REVISIÓN SISTEMÁTICA
El recurso que los autores necesitan es su propio tiempo, la mayoría de los autores aportan su tiempo sin ninguna remuneración económica porque el producto que se logra es mantenerse actualizados en su área de interés. El tiempo que se necesita es variable de acuerdo con el tema de la revisión, el número de estudios, los métodos utilizados.
La atención de las tareas correspondientes y el tiempo requerido para cada una de ellas puede ayudar a los autores a calcular la cantidad de tiempo que necesitarán.
FINANCIAMIENTO
Las organizaciones locales que aporten la financiación de las RS dependerán de que los temas sean prioritarios en las políticas de salud local actual. Se pueden buscar en gobernaciones, alcaldías, organizaciones no gubernamentales, agencias para la financiación de investigación, organizaciones que aportan o financian servicios de salud, responsables que están involucrados en el desarrollo de guías para la práctica clínica y personas particulares que buscan cumplir con el encargo social de su pueblo.
AGENDA PARA UNA RS (según CC)
1. Establecer un tema prioritario que beneficie a la comunidad.
2. Elaboración del protocolo.
3. Búsquedas de estudios publicados y no publicados.
4. Prueba piloto de criterios de elegibilidad.
5. Evaluación de la inclusión de estudios.
6. Prueba piloto de evaluación de "Riesgo de sesgo".
7. Evaluaciones de la validez.
8. Prueba piloto de la extracción de datos.
9. Extracción de datos.
10. Entrada de datos en RevMan.
11. Seguimiento de datos perdidos.
12. Análisis.
13. Preparación del informe de la revisión.
14. Mantenimiento de la revisión actualizada.
La publicación de las RS tiene un canal formal para su publicación, es acudiendo a CC, también se podrán utilizar otras revistas científicas que existen en el medio, particularmente asume enorme importancia el espacio que podrán tener en la Rev. Del Col Med de La Paz, como espacio de publicación.
Es muy importante saber que la CC plantea como única condición para la publicación conjunta: que las RS deben permanecer libres para ser difundidas en cualquier medio, sin restricción de ninguno de ellos. La CC en sus declaración de principios establece que el bien es para todos los ciudadanos del mundo por lo que no firman derechos exclusivos con ninguna revista o editor.
ÉTICA Y CONFLICTOS DE INTERÉS
Una de las fundamentaciones más importantes en lo que se refiere a las RS es el total cumplimento y respeto de todos los derechos de los participantes, no debe haber ningún posibilidad de discriminación y debe estar libre de cualquier sesgo real o aparente debido al recibo de cualquier beneficio en efectivo o en especie, cualquier atención, o cualquier subsidio derivado de cualquier fuente que pueda tener o ser interpretado como susceptible de tener interés en el resultado de la revisión.
Se debe también considerar aspectos, como debe citarse el documento, los autores, participantes, agradecimientos, la presencia de grupos asesores, los procedimientos editoriales y la publicación en sí misma.
RESUMEN PARA LA ELABORACION RS
1. Formulación de la pregunta que defina los pacientes/enfermedad y las intervenciones.
2. Localización de los estudios, se utilizan varias fuentes de búsqueda para la localización e identificación de los estudios relevantes de las principales fuentes electrónicas:
Lilacs, Medline plus, Embase, Cochrane Controlled Trials Database, SciSearch, Scielo, otras fuentes de información como: trabajos publicados en anales de congresos; estudios de especialistas y búsquedas manuales en revistas no disponibles en las bases de datos. Para cada una de esas fuentes utilizadas debe detallarse la estrategia de búsqueda utilizada.
3. Evaluación crítica de los estudios para determinar la validez de los estudios seleccionados. Esa evaluación crítica permite determinar qué estudios serán utilizados en la revisión. Los que no cumplan con los criterios de validez deberán ser citados y explicados acerca del motivo de la exclusión.
4. La recolección de datos y de todas las variables estudiadas deben ser observadas en los estudios y resumidas, además de las características del método, de los participantes y de los desenlaces clínicos, que permitieron determinar la posibilidad de comparar o no los estudios seleccionados.
5. Análisis y presentación de los datos de los estudios deben ser agrupados con base en la semejanza entre los estudios. Cada uno de esos agrupamientos deberá ser preestablecido en el proyecto, así como la forma de presentación gráfica y numérica, para facilitar el entendimiento del lector.
Cuando se ha realizado un método estadístico en el análisis y síntesis de los resultados de los estudios incluidos, puede decirse que se tiene una RS con metanálisis.
6. Se debe realizar la interpretación de los dato, que determinen la fuerza de la evidencia encontrada, la aplicabilidad de los resultados, el costo y la práctica corriente que sean relevantes, determinando claramente los límites entre los beneficios y los riesgos.
7. Una vez publicada, la revisión recibirá sugerencias y críticas que deben ser incorporadas a las ediciones subsecuentes, caracterizando una publicación dinámica que debe ser actualizada cada vez que surjan nuevos estudios en el tema.
8. Estudios de bases de datos administrativas y encuestas comunitarias que ayudan a colocar los problemas en una perspectiva comparativa.
9. Estudios observacionales que ayudan a describir los daños probables de una opción.
10. Estudios cualitativos que ayudan a comprender los significados que los individuos o grupos asignan a un problema, cómo y por qué funcionan las opciones, y los puntos de vista sobre las opciones particulares
CONCLUSIONES
1. La falta de evidencia de un determinado efecto no debe confundirse con la existencia de evidencia científica sobre la ausencia de un determinado efecto.
2. No es útil incluir evidencia científica con un alto riesgo de sesgo en una revisión, aún en los casos en los que la evidencia disponible no es mejor.
3. No es útil centrarse en variables de resultado triviales sólo porque hayan sido escogidas por otros investigadores para hacer las mediciones en estudios individuales.
4. En la medida de lo posible, es importante asumir una perspectiva internacional.
5. La evidencia recopilada no debe estar restringida por nacionalidad o idioma sin una buena razón, la información recogida en los antecedentes sobre la prevalencia y la morbilidad debería ofrecer una visión global, y habría que hacer el esfuerzo de situar los resultados de la revisión en un contexto amplio.
6. Las revisiones Cochrane y los protocolos de revisiones se preparan en el software de la Colaboración Cochrane Review Manager (RevMan), y tienen un formato único, de fácil acceso y sin costo económico.
7. En nuestro país tenemos temas para realizar RS de enorme relevancia que toca diferentes departamentos, por ejemplo, se pueden realizar revisiones sobre chagas, tuberculosis, malaria, dengue, artritis reumatoide, diabetes y muchas otras que están esperando la oportunidad que nos pongamos a trabajar sobre ellas.
8. Asegurarse de que los autores reciban el apoyo metodológico que necesitan.
9. Existen guías clínicas elaboradas y publicadas en base a las mejores evidencias que cumplen con los principios del juramento de Hipócrates.
REFERENCIAS
1. Egger M, Smith GD, Phillips AN. Meta-analysis: Principles and procedures. BMJ 1997; 315: 1533-1537. [ Links ]
2. Ruano-Raviña A, Figueiras A, Barros-Dios JM. El metaanálisis a debate. Med Clin (Barc) 2002; 119(11): 435-439. [ Links ]
3. Effective Public Health Practice Project 2007. Effective Public Health Practice Project [Updated 25 October 2007]. Available from: http://www.city.hamilton.on.ca/PHCS/EPHPP (accessed 1 January 2008). [ Links ]
4. Khan KS, ter Riet G, Glanville J, Sowden AJ, Kleijnen J (editors). Undertaking Systematic Reviews of Research on Effectiveness: CRD's Guidance for those Carrying Out or Commissioning Reviews (CRD Report Number 4) (2nd edition). York (UK): NHS Centre for Reviews and Dissemination, University of York, 2001. [ Links ]
5. Steel R. Involving marginalised and vulnerable groups in research: a discussion document. Consumers in NHS research [2001]. Available from: http://www.invo.org.uk/pdf/Involving_Marginalised_Groups_in_Research.pdf (accessed 1 January 2008). [ Links ]
6. Greenland S. Quantitative methods in the review of epidemiologic literature. Epidemiol Rev 1987; 9: 1-30. [ Links ]
7. Friedenreich CM. Methods for pooled analysis of epidemiologic studies. Epidemiology 1993; 4: 295-302. Abraira V. Revisiones sistemáticas y metaanálisis. Semergen 2003; 29(4): 183-185. [ Links ]
8. Der Simonian R, Laird N. Meta-analysis in clinical trials. Control Clin Trials 1986; 7: 177-188. L'Abbé K, DetskyA, O'Rourke K. Meta-analysis in clinical research. Ann Intern Med 1987; 107: 224-233. [ Links ]
9. Galbraith R. A note on graphical presentation of estimated odds ratios from several clinical trials. Stat Med 1988; 7: 889-894. [ Links ]
10. Egger M, Smith GD, Phillips AN. Meta-analysis: Principles and procedures. BMJ 1997; 315: 1533-1537. [ Links ]
11. Egger M, Smith GD, Schneider M, Minder C. Bias in meta-analysis detect by a simple, graphical test. BMJ 1997; 315: 629-634. [ Links ]
12. Begg CB, Mazumsdar M. Operating characteristics of a rank correlation test for publication bias. Biometrics 1994; 50: 1088-1101. [ Links ]