INTRODUCCION
El descubrimiento de nuevos prototipos con actividad inhibitoria de fosfolipasas A2 (PLA2) es un área de gran interés farmacológico y biotecnológico, orientado a evitar los efectos fisiopatológicos derivados de la acción de las PLA2 a nivel orgánico o derivada de accidentes ofídicos. En este escenario resulta de gran importancia desarrollar investigaciones enfocadas al descubrimiento de moléculas con alta bioactividad, y especificidad, que disminuyan la actividad enzimática de las PLA2. Una molécula bioactiva se convertirá en un modelo para desarrollo de un fármaco si además no presenta toxicidad y es efectiva en el tratamiento de enfermedades cuyo mecanismo de acción involucra a esta enzima (Sales et al., 2017).
Los venenos animales son mezclas de sustancias ricas en moléculas biológicamente activas como proteínas (con y sin actividad enzimática), péptidos, aminas biogénicas y otras, que poseen alta especificidad por una variedad de dianas específicas lo que afecta la fisiología orgánica y la homeostasis celular. (Harvey, 2014; Utkin, 2015). En los venenos de serpientes, alrededor del 90% de sus componentes son de origen proteico (Tasoulis & Isbister, 2017), siendo las PLA2 las enzimas más abundantes. Estas enzimas hidrolizan el enlace éster 2-acílico en los fosfolípidos de membrana liberando lisofosfolípidos y ácidos grasos libres como, por ejemplo, ácidos araquidónico (ARA) u oleico (Calvete, 2013; Dennis et al., 2011; Filkin et al., 2020).
A continuación, se revisarán estudios los cuales han promovido la búsqueda de nuevas moléculas inhibidoras de PLA2, algunos de estos estudios han tomado las PLA2 presente en los venenos de serpientes y posteriormente han sido evaluadas frente a moléculas de origen natural y sintético como inhibidoras de la actividad enzimática. Revisaremos las moléculas y sus grupos funcionales para conocer aquellas con la estructura molecular más promisoria como potenciales inhibidores de la actividad enzimática.
Las enzimas fosfolipasas y fosfolipasas A2: características y funciones
Las fosfolipasas son un grupo de enzimas involucradas en la hidrólisis de fosfolípidos. Hay cinco tipos básicos de fosfolipasas, clasificadas según los sitios de escisión en sustratos de fosfolípidos.
Las fosfolipasas A (PLA) son acil hidrolasas clasificadas según la capacidad de hidrolizar al éster 1-acílico (PLA1) o al éster 2-acílico (PLA2). Las fosfolipasas que hidrolizan ambos grupos acilo se denominan fosfolipasa B (PLB). La escisión del enlace glicerofosfato es catalizada por la fosfolipasa C (PLC), mientras que la eliminación del grupo base es catalizada por la fosfolipasa D (PLD). Por tanto, la PLC y la PLD son fosfodiesterasas (Xuemin, 2018).
La superfamilia de PLA2 está conformada por 16 grupos de proteínas (I-XVI) con masa molecular (de 10 a 114 kDa), divididas en seis subgrupos distintos: PLA2 secretadas (sPLA2), PLA2 citosólicas (cPLA2), PLA2 independientes de calcio (iPLA2), acetilhidrolasas PAF (PAF-AH), lisosomal (LPPLA2) y específica del tejido adiposo (AdPLA2) (Dennis et al., 2011; Filkin et al., 2020; Quach et al., 2014). Las sPLA2 se caracterizan por tener un bajo peso molecular (14-18 kDa), estas isoformas son calcio dependientes y actúan en la sección extracelular de la membrana celular (Batsika et al., 2021; Quach et al., 2014; Zhang et al., 2021).
Las sPLA2 contienen de cinco a ocho enlaces disulfuro y se clasifican en los grupos I, II, III, V, IX, X, XI, XII, XIII y XIV y subgrupos A, B, C, D, E y F. Entre las sPLA2 se incluye las PLA2 de páncreas, líquido sinovial, venenos de serpientes y abejas (Dennis et al., 2011; Magrioti & Kokotos, 2013; Su & Chang, 1984). Estas enzimas se involucran en mecanismos de edema, hemorragia e inhibición de la agregación plaquetaria, así también generan efectos neurotóxicos, anticoagulantes y miotóxicos (Da Silva et al., 2009; Xiao et al., 2017)
Las PLA2 de veneno (sPLA2) presentes en las serpientes están clasificadas en el Grupo I (IA/IB) y Grupo II (IIA/IIB). Esta clasificación se basa en la similitud de secuencia, la posición de los enlaces disulfuro y las inserciones de bucles. Las sPLA2 de serpiente son clasificadas en los grupos IA y IIA, tienen siete enlaces disulfuro: seis de ellos se conservan en las familias Elapidae y Viperidae, mientras que los enlaces disulfuro Cys11 / Cys77 y Cys51 / Cys133 varían respectivamente. Las sPLA2 del grupo IIB, presentes en la familia Crotalidae y Bitis, tienen solo seis enlaces disulfuro, sin el enlace Cys61 / Cys95. Estas enzimas sPLA2 y sus grupos IA y II (IIA y IIB) tiene un sitio catalítico formado por His/Asp y requiere de calcio (Ca2+) para la actividad catalítica, es decir son calcio dependientes (Dennis et al., 2011; Xiao et al., 2017).
PLA2 y su relación con la inflamación
Las PLA2 hidrolizan fosfolípidos de membrana liberando ARA, un precursor de los eicosanoides proinflamatorios (Batsika et al., 2021; Calvete, 2013; Dennis et al., 2011). El ARA liberado se convierte en prostaglandinas (PG), prostaciclinas (PC) por acción de las ciclooxigenasas (COX1 / COX2) y en leucotrienos (LT) por acción de la 5-lipoxigenasa (5-LO). Este proceso se esquematiza en la Figura 1.
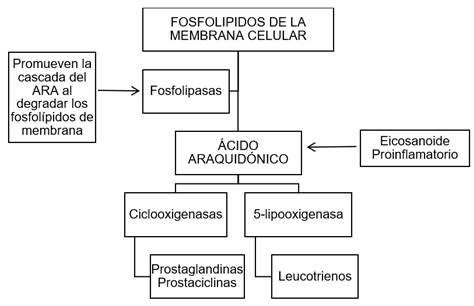
Figura 1 Cascada del ARA por acción de las COX y 5-LO con la formación de eicosanoides proinflamatorios
Los AINEs inhiben las COX1 y COX2 reduciendo la síntesis de PG y PC, pero no inhiben la acción de 5-LO (De Angelis &Tata, 2016). Así, el ARA producido mediante la acción de la 5-LO será convertido en LT, que en altas concentraciones está directamente relacionado con efectos adversos en el tracto gástrico y renal. Se estima que, desarrollar un fármaco inhibidor selectivo de las PLA2, podría ser una buena estrategia para evitar, no solo la formación de PG y PC, sino también la formación de LT y, así, evitar todos sus efectos secundarios pues se inhibiría el primer paso de la cascada del ARA (Sales et al., 2017).
Respecto a la regulación de la expresión de sPLA2 por señalización celular y regulación génica, los productos de degradación de la escisión de los fosfolípidos (ARA y lisofosfolípidos=LP) por sPLA2 y cPLA2 pueden metabolizarse más a segundos mensajeros de señalización (Ácido lisofosfatídico=LPA, PG, LT) para desencadenar vías de señalización celular activando receptores acoplados a proteína G (GPCR) y receptores de citocinas. Estos eventos resultan en la amplificación de la producción de citocinas proinflamatorias y la intensificación de la inflamación. (Quach et al., 2014).
La desregulación de la actividad enzimática de las sPLA2 conducen a la generación de ARA en diferentes tejidos afectados (cardíaco, nervioso, respiratorio, pancreático, hepático, articular, digestivo, etc.), lo cual conduce a trastornos inflamatorios como sepsis, asma, enfermedad de Alzheimer, aterosclerosis, entre otros (Alasmary et al., 2017). Estas patologías aumentan la expresión de las isoformas de sPLA2, lo que aumenta la liberación de ARA a niveles tres veces mayores que los niveles basales, entonces el ARA se metaboliza en las células a través de la COX y la 5-LO para producir mediadores proinflamatorios como PG y LT, respectivamente. Estos pueden estimular la producción de citocinas inflamatorias, incluido el factor de necrosis tumoral alfa (TNF-α) y las interleucinas (IL), lo que lleva a la amplificación de la señal y la intensificación del evento inflamatorio y estrés oxidativo (Quach et al., 2014). La elevación crónica de la glucosa en sangre conduce a una mayor activación de sPLA2, generación de ARA y eicosanoides y cardiopatía coronaria inflamatoria. Se han estudiado varias isoenzimas sPLA2 por su implicación en la regulación de la glucosa en sangre a través de mecanismos insulinodependientes. Estas enzimas también están involucradas en las complicaciones cardiovasculares de la diabetes (Hui, 2012) . Así, la sPLA2 del grupo IB promueve la resistencia a la insulina y la hiperglucemia en ratones transgénicos que sobre expresan esta enzima. El grupo X sPLA2 es otro regulador de la producción de insulina, donde suprime la secreción de insulina estimulada por glucosa de las células beta a través de un mecanismo dependiente de COX-2 (Shridas et al., 2014). Se encontró que los sujetos diabéticos eran más susceptibles a la lipólisis por el grupo V sPLA2 aumentando su estado de inflamación y aumentando su riesgo de complicaciones cardiovasculares (Alasmary et al., 2017).
Moléculas naturales y sintéticas, candidatas a inhibidoras de sPLA2
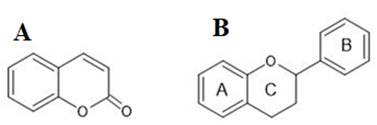
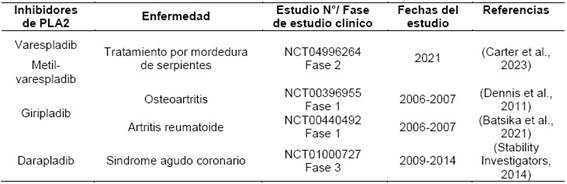
Encontrar nuevos prototipos terapéuticos mediante análisis in vitro se muestra como una alternativa para la síntesis y bioensayos in vivo racionales de nuevas moléculas. Se han estudiado compuestos con actividad inhibitoria frente a PLA2 con estructuras moleculares de tipo flavonoide (Carvalho et al., 2013), incluyendo a cumarinas ya que el anillo benzopirano es una estructura común e intermedia en la síntesis de flavonoides y cumarinas, además están ampliamente ligadas al tratamiento de enfermedades inflamatorias, en donde, el farmacóforo ligado a la acción antiinflamatoria es el anillo benzopirano, el mismo que presenta actividad anti sPLA2 mediante inactivación del canal hidrofóbico de la enzima mencionada. Se muestran estructuras generales de estos dos tipos de moléculas en la Figura 2.
MATERIALES Y MÉTODOS
Búsqueda bibliográfica de compuestos con actividad enzimática inhibitoria de sPLA 2
Con el fin de explorar las características estructurales de moléculas inhibitorias de enzimas sPLA2, se llevó a cabo una búsqueda bibliográfica. En esta revisión se incluyeron compuestos que reportaron actividad inhibitoria “in silico” e “in vitro”, explorando las principales bases digitales tales como el Centro Nacional de Información Biotecnológica (NCBI), Google Scholar, y PubMed. Se incluyeron artículos comprendidos desde el año 2011 a 2021 y se revisaron un total de 26 estudios acerca de la inhibición de sPLA2.
Como las PLA2 (sPLA2, cPLA2 y LPLA2) están relacionadas a diversas enfermedades inflamatorias, autoinmunes, cancerígenas, respiratorias, cardíacas, infecciosas, endocrinas, entre otras; un gran número de investigadores vienen trabajando en la búsqueda y desarrollo de inhibidores de la PLA2 como agentes terapéuticos o preventivos, tanto en enfermedades orgánicas, como tratamiento de accidentes ofídicos (Pedada et al., 2016).
Las moléculas con actividad inhibitoria frente a la enzima sPLA2 fueron analizadas con la finalidad de identificar características estructurales relacionadas con la bioactividad observada. Para el efecto, se compararon los patrones de sustitución, tipos y características electrónicas de los sustituyentes, y a partir de esta revisión se identificaron rasgos estructurales característicos, con el fin de guiar nuevos procesos de síntesis de moléculas promisorias ante este blanco farmacológico.
RESULTADOS Y DISCUSIÓN
Varios inhibidores de PLA2 han sido estudiados en el período abordado en esta revisión de literatura, y algunos se han evaluado a nivel de ensayos clínicos para diversas enfermedades inflamatorias y oncológicas, los cuales se reportan en la Tabla 1.
Nuevas moléculas inhibidoras de fosfolipasa A2
Los estudios revisados incluyen ensayos de compuestos naturales y sintéticos que demuestran la actividad inhibitoria frente a sPLA2 de novedosas moléculas cuyas estructuras se presentan a continuación en la Tabla 2.
Tabla 2 Moléculas representativas clasificadas en productos naturales y sintéticos con actividad inhibitoria frente a sPLA2 recopiladas de la literatura.
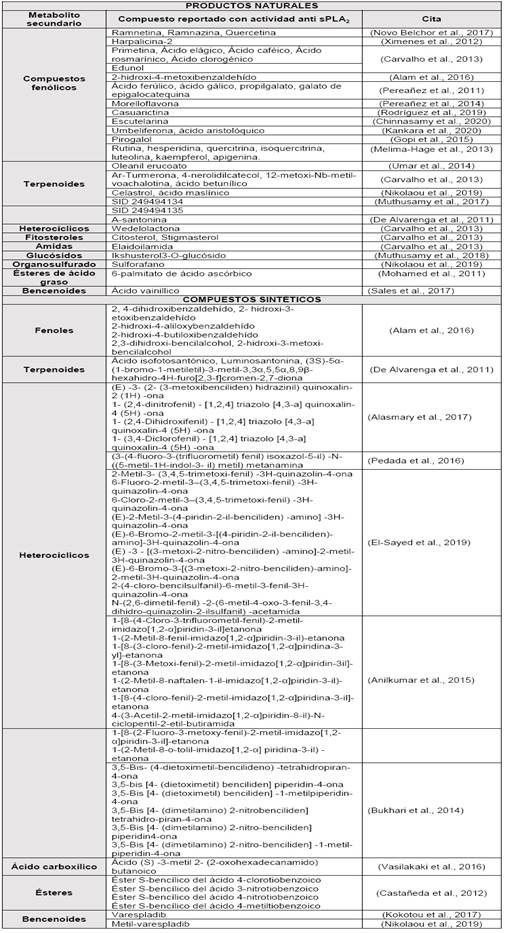
93 compuestos con actividad inhibitoria frente a sPLA2 fueron clasificados según su origen: natural y sintético. Entre las moléculas de origen natural se encuentran compuestos fenólicos, terpenoides, heterocíclicos, fitosteroles, amidas, glucósidos, organosulfurados, ésteres de ácido graso y bencenoides. Las moléculas sintéticas incluyen compuestos fenólicos, terpenoides, heterocíclicos, amidas, ésteres y bencenoides.
La Tabla 2 muestra una gran diversidad estructural de moléculas naturales y sintéticas, promisorias por su capacidad inhibitoria de la enzima sPLA2. (Carvalho et al., 2013; Chinnasamy et al., 2020; Melima-Hage et al., 2013; Novo Belchor et al., 2017; Pereañez et al., 2014; Ximenes et al., 2012).
Existen datos de cumarinas inhibidoras de PLA2 como en el estudio de Fonseca et al., 2010 en el cual se evidenció que el 2-oxo-2H-cromen-3-carboxilato de etilo (EOCC), una cumarina sintética, inhibe irreversiblemente la fosfolipasa A2(sPLA2) del veneno deCrotalus durissus ruruima. En el estudio de Toyama et al., 2009 se reporta el efecto de la umbeliferona (7-hidroxicumarina, 7-HOC) que interactúa con sPLA2 del veneno de Crotalus durissus collilineatus y causa algunas modificaciones estructurales que conducen a una fuerte inhibición de la actividad de esta enzima. Nargotra et al., 2011 realizaron estudios in silico, identificando 27 estructuras cumarínicas como posibles inhibidores de la sPLA2 de Vipera russelli.
En el estudio de Carvalho et al., 2013, se demuestra que los flavonoides ejercen su efecto inhibidor a través de interacciones hidrofóbicas con los anillos A y B y residuos de aminoácidos aromáticos o hidrofóbicos en la proteína. En el trabajo de Novo Belchor et al., 2017, se evaluó la Quercetina (Q) y sus derivados metilados ramentina (Rhm), ramnazina (Rhz) y 3-O-metilquercetina (3MQ) con el objetivo de buscar nuevos compuestos capaces de inhibir la acción de la enzima PLA2. En este ensayo se utilizó sPLA2 de Bothrops jararacussu y se evidenció que, entre las quercetinas metiladas, Rhz exhibió mayor inhibición que 3MQ y Rhm. La actividad inhibitoria de Rhz fue similar a Q. A pesar de que Rhz mostró metilación en el anillo A y el anillo B, la presencia de 3-OH en el anillo C fue probablemente un grupo común en los flavonoles Rhm, Rhz y Q, lo que lleva a la inhibición de sPLA2. Sin embargo, Rhz exhibe una mayor inhibición que Rhm debido a la presencia del grupo metilado en el anillo B. Se observó una mayor interacción con sPLA2 en Q, exhibiendo mayor inhibición entre las quercetinas estudiadas. El análisis de los resultados de este estudio mostró que el reemplazo del grupo OH en el anillo C por un grupo metilo abolió casi por completo la capacidad inhibidora de 3MQ frente a sPLA2.
Así mismo, las moléculas tipo flavonoide, reportadas en nuestra revisión de literatura no exhiben metilación en el anillo C (Carvalho et al., 2013; Chinnasamy et al., 2020; Melima-Hage et al., 2013; Novo Belchor et al., 2017; Pereañez et al., 2014; Ximenes et al., 2012). Este rasgo estructural se muestra relevante en la actividad inhibitoria frente a la enzima sPLA2.
El mecanismo inhibitorio implica el ataque nucleofílico de los residuos de aminoácidos y la unión al gran bolsillo hidrofóbico de la sPLA2. La pérdida de la integridad de la bolsa hidrofóbica induce una pérdida irreversible de la actividad enzimática. En consecuencia, todos los efectos biológicos que dependen de la actividad catalítica de sPLA2 quedan virtualmente abolidos. Dado que la estabilidad de la hélice alfa en la cavidad hidrofóbica debería verse afectada por la estabilidad de otras estructuras, como el bucle de unión al calcio o el ala beta, es posible que los efectos farmacológicos inducidos por la interacción de sPLA2 con el receptor se vean afectados. Esta hipótesis está fuertemente respaldada por estudios de sPLA2 modificados con otros compuestos polifenólicos (Iglesias et al., 2005; Toyama et al., 2009), así como por otros estudios (Harper and Powers, 1985; Liu et al., 2008). Podemos decir que los efectos farmacológicos de compuestos polifenólicos derivados de plantas relacionados, como cumarinas, flavonoides, terpenoides y alcaloides tienen capacidad inhibitoria frente a sPLA2.
Es importante destacar que, entre las moléculas bioactivas reportadas en nuestra revisión bibliográfica no se encuentran compuestos con sustituyentes halógenos en el anillo B (Carvalho et al., 2013; Chinnasamy et al., 2020; Melima-Hage et al., 2013; Novo Belchor et al., 2017; Pereañez et al., 2014; Ximenes et al., 2012). Estos hallazgos indican que el efecto inductivo ejercido por el sustituyente, debido a su elevada electronegatividad, genera un impedimento al anillo B y causa la pérdida de actividad anti sPLA2.
Un cambio de posición del anillo B genera un impedimento estérico, inactivando las moléculas ante la enzima sPLA2. Este impedimento estérico cambia la estructura tridimensional de la molécula, lo cual puede afectar en la unión de esta al sitio activo de la enzima.
El conocimiento recopilado del análisis del mecanismo de acción y características estructurales de inhibidores de sPLA2 permitirá plantear estudios de relaciones estructura - actividad, orientados a seleccionar moléculas candidato para el desarrollo de fármacos con mejor actividad y menos efectos secundarios, para el tratamiento del dolor y procesos inflamatorios.
CONCLUSIÓN
En el presente trabajo se reportan compuestos de origen natural y sintético que interactúan con el sitio catalítico de la enzima sPLA2 conformado por His/Asp. La revisión de literatura se encaminó a la búsqueda de compuestos que interactúen con estas enzimas en específico, ya que otras PLA2 tienen sitios catalíticos diferentes y por tanto el mecanismo de acción puede variar. Así, los compuestos reportados han demostrado su afinidad por sPLA2.
El análisis de las características estructurales de estos compuestos permite determinar que la actividad anti sPLA2 puede asociarse a los patrones de sustitución en el anillo bencénico. Esto se desprende de la comparación de las moléculas reportadas en esta revisión. Adicionalmente se evidenció que los compuestos con sustituyentes nitrogenados podrían exhibir mayor actividad, ya que ejercen un efecto no inductivo, al ceder sus cargas pueden unirse con mayor facilidad al sitio activo de la enzima. No obstante, se recomiendan estudios a futuro con este tipo de moléculas y sustituyentes nitrogenados mediante estudios de relación estructura actividad a fin de encontrar compuestos mucho más eficaces y modelos químicos que permitan la síntesis de nuevos compuestos para la inhibición de estas enzimas.












 uBio
uBio